Química del diòxid de sofre al vi
Dr. Enginyer Mario Ignacio Weibel, responsable I+D+r Tecnología Difusión Ibérica S.L.
El diòxid de sofre, anhídrid sulfurós o simplement SO2 és l’additiu més àmpliament utilitzat a la indústria vitivinícola. La seva utilització a la indústria alimentària en general, i vinícola en particular, data de l’època romana i ha rebut diferents qüestionaments al llarg de la història. Si bé l’absència de SO2 al vi pot generar diversitat de problemes microbians i pèrdues d’aroma i color, una dosi excessiva també pot provocar alteracions en l’aroma i el sabor del vi i fins i tot podria arribar a ser perjudicial per a la salut del consumidor. Els sulfits són particularment perillosos per a aquelles persones intolerants que no tenen l’enzim necessari per a la seva degradació (sulfit oxidasa), podent provocar-los dermatitis, urticària, dolor abdominal, diarrea i vòmits. També és problemàtic per a les persones que pateixen d’asma, per què poden generar complicacions com ara broncoconstricció i augmentar la gravetat dels símptomes.
A nivell europeu, la ingesta diària admissible està fixada a 0,7 mg/kg del pes corporal. Per aquests motius, els nivells màxims admissibles de SO2 estan determinats per llei a la majoria dels països. En el cas de la Unió Europea, el Reglament Delegat 2019/934 de la Comissió marca els continguts màxims a SO2 permesos, com es mostra a la Taula 1.
 Taula 1. Continguts màxims de SO2 Total (mg/L) permesos a la UE.
Taula 1. Continguts màxims de SO2 Total (mg/L) permesos a la UE.
En el cas de vins ecològics, el Reglament d’Execució 203/2012 de la Comissió fixa que quan el contingut de sucre residual és menor a 2 g/L, els límits són de 100 mg/L SO2 per a negres i 150 mg/L per a blancs i rosats. Per a la resta de vins, s’ha de reduir en 30 mg/L el límit màxim mostrat a la Taula 1. Els vins secs biodinàmics certificats per Demeter tenen un límit fixat en 70 mg/L SO2 per a negres i 90 mg/L per a blancs i rosats. 167 / 5.000 Resultats de traducció Resultat de traducció Per a vins naturals secs, els límits estan fixats en 30 mg/L SO2 per a negres i 40 mg/L per a blancs i rosats (segons l’Association des Vins Naturels, de França). D’altra banda, la legislació actual d’etiquetatge de productes vitícoles obliga a declarar la presència de SO2 quan les concentracions són superiors a 10 mg/L en termes de SO2 Total.
La tendència actual a la reducció dels nivells de SO2 fa que al mercat es puguin trobar vins sense sulfits afegits. Però, això no implica que no continguin sulfits en absolut. De fet, és molt difícil obtenir un vi sense sulfits. Això és perquè el propi llevat responsable de la fermentació alcohòlica produeix naturalment SO2 i l’allibera al medi. El raïm absorbeix, a través de l’arrel, els sulfats provinents del terra. En absència d’oxigen, els llevats poden reduir els sulfats del most: en una primera etapa a sulfits i en una segona etapa a sulfurs, necessaris per a la síntesi d’aminoàcids sofrats. En alguns casos, l’enzim responsable de reduir els sulfits s’altera, per tant, aquests s’acumulen a l’interior de la cèl·lula i s’acaba alliberant SO2 al medi. D’altra banda, finalitzada la fermentació i durant el repòs del vi, els sulfurs es poden tornar a oxidar a sofre i finalment a sulfits. Alguns llevats són capaços de produir major quantitat de SO2 que altres, per la qual cosa els ceps es classifiquen en llevats de baixa i alta producció. Actualment, la majoria dels llevats comercials poden anomenar-se de baixa producció, ja que els seus nivells de SO2 no superen els 20 mg/L.
Hi ha diversos compostos autoritzats com a additius alimentaris (es reconeixen per estar descrits amb la lletra E seguida d’un nombre) que s’utilitzen per afegir SO2. Aquestes substàncies permeses van des de l’E220 a E228, i són: diòxid de sofre (E220), sulfit de sodi (E221), bisulfit de sodi (E222), metabisulfit de sodi (E223), metabisulfit de potassi (E224), sulfit de potassi (E225), sulfit de calci (E226), bisulfit de calci (E227) i bisulfit de potassi (E228). A nivell enològic, les pràctiques autoritzades permeten únicament la utilització de diòxid de sofre (E220), metabisulfit de potassi (E224) i bisulfit de potassi (E228). A més, només durant la fermentació alcohòlica, es pot emprar bisulfit d’amoni com a activador.
Efectes i propietats
Tres grans propietats que se li atribueixen al SO2 són el seu poder antioxidant, antioxidàsic i antimicrobià. L’acció antioxidant es deu al consum de l’oxigen dissolt i del peròxid d’hidrogen que pogués ser present i la reducció de les quinones a la forma fenòlica. El poder antioxidàsic es fonamenta en la capacitat del SO2 d’inhibir enzims com la polifenol oxidasa, principal responsable del pardejament al vi. L’efecte antimicrobià s’explica per un bloqueig del complex enzimàtic dels microorganismes, podent portar a la inhibició del creixement o fins i tot la mort. En general, es considera que el SO2 és més efectiu contra bacteris que contra llevats, sent important la seva acció davant de bacteris làctics i llevats del gènere Brettanomyces. El SO2 també presenta poder disgregant per la seva capacitat de trencar la paret cel·lular de la pell del raïm, permetent una ràpida extracció dels components al most. Per acabar, el SO2 té cert poder clarificant a causa de la capacitat de destruir els col·loides protectors del raïm (pectines, gomes, mucílags), facilitant la precipitació de les partícules i evitant la formació de terbolesa.
Formes químiques del SO2
Totes les propietats que s’adjudiquen al SO2, depenen fonamentalment de la concentració i la forma en què aquest es trobe dissolt al most o vi. No totes les formes del SO2 són igual d’actives per dur a terme les funcions. Quan qualsevol dels additius abans esmentats s’agreguen al most o vi, el SO2 reacciona amb l’aigua formant una varietat de substàncies que estaran en un complex equilibri químic.
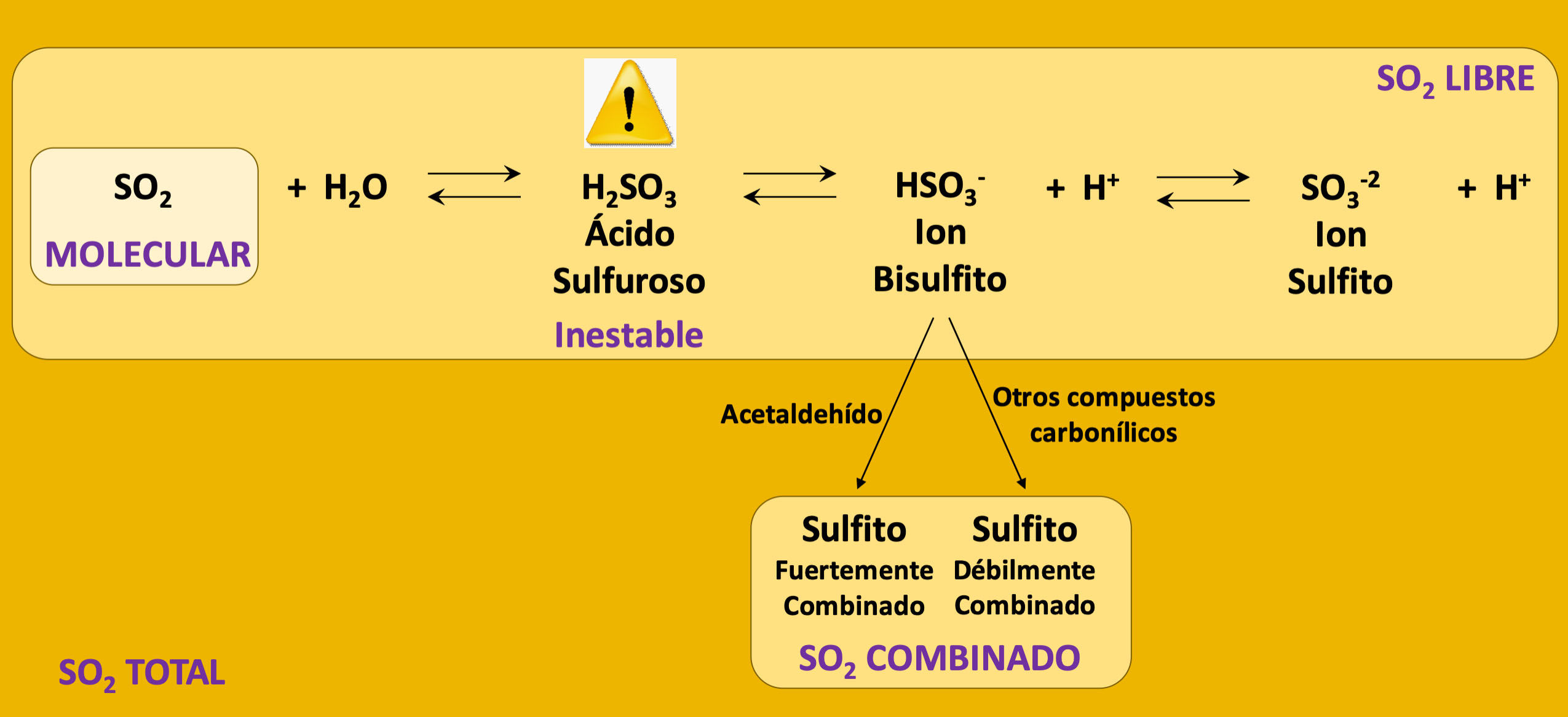
 Figura 1. Equilibri esquemàtic de les formes químiques del SO2 presents al vi.
Figura 1. Equilibri esquemàtic de les formes químiques del SO2 presents al vi.
A la Figura 1, podem observar detalladament les diferents formes químiques del SO2. Aleshores es poden distingir cinc formes per al SO2 en solució: el SO2 Molecular, l’ió bisulfit (HSO3-), l’ió bisulfit (SO3-2) i les formes combinades del SO2 (l’àcid sulfurós, H2SO3, és massa inestable per ser detectat en solució). Les tres primeres formes químiques componen l’anomenat SO2 Lliure, mentre que les dues últimes generen l’anomenat SO2 Combinat. La suma del SO2 Lliure i el combinat dóna el valor de SO2 Total, que és el paràmetre utilitzat com a referència als límits màxims fixats per la legislació.
A aquestes cinc formes en solució, se li podria afegir el SO2 gasós que es troba als espais d’aire dels tancs o a l’espai del cap de l’ampolla i que està en equilibri amb el SO2 Molecular. A continuació, descriurem més detalladament cadascuna.
SO2 Lliure
El SO2 Molecular és el responsable de l’acció antisèptica. S’acostuma considerar que és 20 vegades més efectiu que l’ió bisulfit en la inhibició de llevats i 500 vegades més en la inhibició de bacteris. A més, té certa activitat antioxidant. Per la seva banda, l’ió bisulfit és el principal responsable de la inhibició de la polifenol oxidasa, i és menor la seva activitat antioxidant i antimicrobiana. Finalment, l’ió sulfit és capaç de reaccionar amb l’oxigen i el peròxid d’hidrogen dissolt, i per tant té certa capacitat antioxidant. Aquestes tres formes químiques formen el denominat SO2 Lliure, fonamental en el control del vi. La concentració relativa de cadascuna de les tres formes químiques estarà determinada per les constants químiques de dissociació (K1 per a l’equilibri entre SO2 Molecular i ió bisulfit i K2 per a l’equilibri entre ió bisulfit i ió sulfit) i el valor de pH, pel seu efecte en la concentració d’ions hidrogen al medi.

Figura 2. Equilibri entre les formes químiques del SO Lliure en funció del pH del medi.
La Figura 2 mostra levolució de la concentració de les diferents formes segons el valor de pH del medi. Es pot observar que als valors de pH habituals en vi (entre 3 i 4), la forma bisulfit és pràcticament majoritària mentre que la forma sulfit és gairebé menyspreable. Per tant, el pH no influirà la funció antioxidàssica. D’altra banda, la presència de SO2 Molecular, responsable de l’activitat antimicrobiana, és més gran a pH més baixos (més àcids). A tall d’exemple, a un pH igual a 3, el SO2 Molecular representa el 5,9% mentre que a un pH igual a 4 només representa el 0,6%, unes deu vegades menys, quedant per tant molt limitada la seva acció antisèptica. Una manera ràpida d’estimar el SO2 Molecular present al nostre vi és utilitzar taules que brinden la concentració del mateix en funció del pH i del valor de SO2 Lliure. Una altra manera és utilitzar la fórmula matemàtica següent.

Pel que fa al nivell de protecció antimicrobiana necessària, s’acostumen recomanar nivells de 0,5 mg/L de SO2 Molecular per a vins negres secs, 0,8 mg/L per a vins blancs secs i 2 mg/L per a vins dolços. Tenint en compte aquests nivells recomanats, a la Taula 2 es pot observar el nivell de SO2 Lliure necessari en funció del pH per arribar a aquest nivell de protecció.

Taula 2. Contingut de SO2 Lliure (mg/L) necessari per obtenir una certa dosi de SO2 Molecular.
Si prenem com a exemple un vi blanc sec amb pH de 3,20, es necessitarien 21 mg/L de SO2 Lliure per obtenir la protecció necessària. Si en canvi fos un vi negre sec amb un pH lleugerament àcid de 3,50 caldrien 26 mg/L de SO2 Lliure. Si aquest mateix vi negre tingués un pH més elevat, per exemple de 3,80, passarien a ser necessaris 51 mg/L de SO2 Lliure, aproximadament el doble. I si, per desgràcia, el pH fora de 4, la dosi requerida de SO2 Lliure seria de 80 mg/L. Per tant, es pot veure la forta influència del pH en la dosi necessària per obtenir una protecció antimicrobiana efectiva.
Tots els càlculs fets abans estan realitzats a una temperatura de 20 °C i en un medi totalment aquós. Tot i això, el vi és una barreja molt complexa de diverses substàncies (aigua, alcohol, sucres, etc.). Podria elevar-se el nivell de l’anàlisi química a un model més detallat i complet, tenint en compte la influència de la temperatura, el grau alcohòlic i la força iònica sobre el valor de les constants de dissociació K1 i K2, abans anomenades. Hi ha equacions, de certa complexitat, que permeten calcular els valors modificats de les constants en funció de la força iònica, la temperatura i la constant dielèctrica del medi (que depèn alhora de la temperatura, la força iònica i la concentració de les diverses substàncies del medi).

Figura 3. Variació del valor de la pK1 en funció de la temperatura i el grau alcohòlic.
La Figura 3 mostra una de les gràfiques que es poden obtenir a partir d’aquests càlculs. La força iònica té una correlació negativa amb el SO2 Molecular, però es pot considerar menyspreable davant els efectes de la temperatura i el grau alcohòlic. En molts càlculs, se sol prendre un valor de força iònica constant i igual a 0,038 per a tots els vins i mosts. Per la seva banda, la temperatura exerceix el major efecte: un increment de la mateixa eleva el contingut de SO2 Molecular. Com a exemple, un vi de 10° d’alcohol i pH igual a 3,30 tindrà un 4% de SO2 Molecular a 20 ºC, però aquesta proporció s’elevarà a un 14,3% si la temperatura és de 40 ºC. El grau alcohòlic per la seva banda també té un efecte positiu al SO2 Molecular, encara que menor al de la temperatura. Prenent el mateix vi descrit anteriorment a 20°C i pH 3,30, si ara el nivell d’alcohol fos de 15°, la fracció de SO2 Molecular s’elevaria al 4,9%. Hi han diverses taules a la normativa OIV-MA-AS323-04C que permeten calcular el nivell de SO2 Molecular, en funció del pH del vi, el grau alcohòlic, la temperatura i el nivell de SO2 Lliure. Com que l’ús de taules pot resultar tediós, hi ha diverses eines online per facilitar el càlcul per adquirir un cert nivell de protecció de SO2 Molecular, sobre la base dels paràmetres ja esmentats.
SO2 Combinat
El SO2 Combinat es forma per la combinació química de l’ió bisulfit amb diversos compostos presents al most o vi. El SO2 Combinat no posseeix activitat antioxidant i antioxidàsica, i el seu efecte antimicrobià és gairebé menyspreable. Per tant, la combinació del SO2 genera una pèrdua de beneficis derivats del agregat de qualsevol dels productes autoritzats.
Mentre que algunes unions són molt estables, com la generada amb l’acetaldehid, d’altres són relativament poc estables com les establertes amb sucres, àcids cetònics, àcids urònics i antocians. Si s’anomena R el compost amb el qual s’uneix l’ió bisulfit, podem escriure l’equilibri químic i el corresponent constant de dissociació Kd (notar que és la inversa de la constant d’unió).

Si s’anomena R el compost amb el qual s’uneix l’ió bisulfit, podem escriure l’equilibri químic i el corresponent constant de dissociació Kd (notar que és la inversa de la constant d’unió).2, es pot obtenir la següent expressió, que relaciona la forma lliure (RL) i la forma combinada (RC) del compost químic que s’uneix a l’ió bisulfit amb el valor del SO2 Lliure en mg/L.

Prenent una dosi de 20 mg/L de SO2 Lliure, s’analitza l’efecte del valor de Kd. Si Kd és igual o menor a 3 x 10-6 M, la relació RC/RL pren un valor de 105, és a dir, existirà gairebé 100 vegades més compost químic R en la forma combinada que en la forma lliure. Aquest tipus dʻunions generen el SO2 fortament combinat. D’altra banda, si Kd és igual o major a 3 x 10-2, la relació RC/RL pren un valor d’1/100, és a dir, hi ha gairebé 100 vegades més compost químic R en la forma lliure que en la combinada. Aquest tipus d’unions generen el SO2 dèbilment combinat. Quan part del SO2 Lliure s’oxida, aquest tipus d’unions làbils es trenquen per recompondre l’equilibri químic de totes les espècies presents. Per tant, es pot considerar el SO2 feblement combinat com una mena de reserva de SO2 per mantenir la protecció antioxidant. La mateixa anàlisi es pot fer per a diferents concentracions de SO2 Lliure i obtenir el SO2 Combinat coneixent la concentració del compost combinant R, aprofitant que la suma de RC i RL és igual a la concentració del mateix.

Taula 3. Valors de Kd i concentracions mitjanes esperades per a compostos seleccionats.
Reprenent l’equació d’equilibri químic, s’observa que la capacitat de formar compostos de combinació amb l’ió bisulfit depenen de la concentració del compost i del valor de la Kd. A la Taula 3 es detallen els valors de Kd per a diferents compostos presents al vi i les concentracions normalment trobades dels mateixos. L’acetaldehid presenta un valor molt petit de Kd, la qual cosa implica que més del 99% estarà combinat amb l’ió bisulfit, sent un dels principals responsables del SO2 Combinat. Altres compostos importants en analitzar la combinació del SO2 són l’àcid pirúvic i l’àcid 2-oxoglutàric, particularment presents en mosts botrititzats i vins dolços. Altres compostos carbonílics capaços de combinar-se amb l’ió bisulfit són els sucres (particularment, glucosa en mosts i vins dolços), àcids urònics (com el glucurònic i el galacturònic), productes d’oxidació dels sucres (per ex., la 5-oxofructosa) i les lactones de l’àcid glucònic. També l’ió bisulfit es pot combinar amb compostos fenòlics, principalment antocianines, generant una reacció reversible de decoloració del most o vi.
Considerant els valors de Kd i les concentracions normals al vi, es pot arribar a la conclusió que els principals compostos que participen en la formació del SO2 Combinat són, en ordre d’importància, l’acetaldehid (51-76%), l’àcid pirúvic (10-18%), l’àcid 2-oxoglutàric (7-24%) i l’àcid galacturònic (2-11%). En vins dolços, la glucosa passa a ser també un paràmetre que cal tenir en compte (1-2%).

Figura 4. Relació entre el contingut de SO2 Lliure i SO2 Combinat.
Finalment, de l’equació de l’equilibri químic, se’n deriva que el nivell de SO2 Lliure també exerceix influència sobre la quantitat d’ió bisulfit que es combina. Un exemple d’aquesta influència s’observa a la Figura 4, construïda sobre la base de l’àcid pirúvic a una concentració de 88 mg/l (10-3 mol/l). La imatge representa una típica corba de saturació. Això implica que per aconseguir passar de 0 a 20 mg/L de SO2 Lliure, se sacrificaran 33 mg/L de SO2 Combinat. No obstant això, per passar de 20 a 40 mg/L de SO2 Lliure, només se sacrifica un addicional de 10 mg/L de SO2 Combinat. Això és perquè cada vegada queda menys combinant disponible en forma lliure i el principi de la llei d’acció de masses limita la reacció química de combinació.
CONCLUSIONS
La utilització del SO2 en enologia és una pràctica tradicional i àmpliament difosa. Tanmateix, constantment sorgeixen advertiments sobre el seu ús, particularment tenint en compte els efectes adversos sobre la salut humana. Això ha obligat a una revisió creixent sobre la seva ocupació i la reducció en les dosis emprades. Es fa fonamental conèixer la química que s’amaga darrere del SO2 per poder entendre els fenòmens que es produeixen en el vi i així optimitzar les quantitats aplicades.
L’objectiu d’aquest treball és intentar aportar una mica de claredat, brindant eines senzilles per explicar i descriure les diferents formes químiques del SO2 presents al most i al vi. En base a aquest coneixement, i recordant el rol que cada forma química juga en la protecció del vi, es pot preveure la dosi necessària per obtenir una acció antimicrobiana, antioxidant i antioxidàsica adequada.
La base per aplicar les eines disponibles és una correcta determinació del SO2 al vi, tant en la seva forma lliure com total. Des de Tecnologia Difusió Ibèrica, S.L., estem sempre al servei del client, brindant diferents solucions analítiques per a la determinació del SO2, des de valoradors manuals i automàtics basats en el mètode Ripper fins a reactius colorimètrics adaptats per a analitzadors automàtics.
Per a més informació podeu posar-vos en contacte amb nosaltres. Disposem de tota una xarxa comercial desplegada pel territori nacional.