Àcid acètic i acidesa volàtil
Similituds, diferències i mètodes de mesura
Dr. Enginyer Mario Ignacio Weibel, responsable I+D+r Tecnología Difusión Ibérica S.L.
Introducció
L’àcid acètic és un àcid orgànic de cadena curta, que presenta una aroma característica a vinagre, producte del qual forma part en concentracions relativament elevades (4060 g/L). És només un dels diversos àcids que formen part de la composició química del vi: a la suma de tots ells se la coneix com a acidesa total, paràmetre fonamental per saber si un vi tindrà prou cos, si estarà equilibrat i si podrà ser sotmès a processos de criança. L’acidesa total és, alhora, la suma de dos tipus d’acidesa més: la fixa i la volàtil. L’acidesa fixa és, de manera resumida, la suma de tots els àcids que, quan el vi és sotmès a calor, no s’evaporaran. A aquest grup pertanyen els àcids tartàric, màlic, làctic i cítric. La seva presència es nota de manera característica a través del paladar. D’altra banda, l’acidesa volàtil és aquella que es desprendrà del vi en escalfar-lo. A aquest apartat pertanyen els àcids acètic, propiònic i butíric, entre d’altres. L’àcid sòrbic, el diòxid de carboni i el diòxid de sofre també són volàtils, però no s’han de tenir en compte durant la determinació de l’acidesa volàtil. A diferència de l’acidesa fixa, l’acidesa volàtil generalment es nota de manera característica a través del nas.

FOTO: Miura Micro.
En termes generals, es pot considerar que l’àcid acètic i les sals són responsables d’entre un 95% i un 99% de l’acidesa volàtil. D’aquí que usualment se senti parlar de tots dos paràmetres indistintament, encara que químicament això sigui erroni. D’altra banda, quan es parla de sals de l’àcid acètic, se sol referir més específicament a l’acetat d’etil, originat per l’esterificació de l’àcid acètic amb l’etanol present al vi, i que té una forta influència sobre l’aroma.
El contingut normal d’àcid acètic per a un vi ronda els 0,60 g/L mentre que la seva presència comença a notar-se per sobre de 0,700,80 g/L. La legislació local de cada país és la que determina els nivells màxims d’àcid acètic encara que, com a referència, l’OIV ha establert límits d’acidesa volàtil de 1,20 g/L excepte per a vins amb condicions particulars de producció o criança. D’altra banda, si bé l’acetat d’etil aporta poc a la mida de l’acidesa volàtil (hi ha 1 part cada 510 parts d’àcid acètic), té grans connotacions en l’aroma del vi a causa del baix llindar de detecció (0, 08 g/L) i que en altes quantitats aporta aromes desagradables a cola o adhesius.
Per tot això molts historiadors del vi consideren que la determinació de l’acidesa volàtil i l’àcid acètic ha estat el primer paràmetre de qualitat instituït per la indústria vinícola. Abans d’entrar en els mètodes de determinació, però, caldrà entendre com arriba l’àcid acètic a ser un component del vi.
Producció de l’àcid acètic
En general, l’àcid acètic no sol ser present als raïms sans. Tot i això, en aquelles baies “tocades” sí que poden existir concentracions detectables per la qual cosa pot transformar-se en un paràmetre indicador de la qualitat i estat sanitari del raïm en entrar al celler. Els raïms que han patit ruptures de la pell, bé sigui per la calamarsa o per l’acció d’aus i/o insectes, es poden veure infectats a la polpa per diversos fongs i bacteris. Així, en raïms afectats per Botritys, s’han detectat poblacions anormalment altes de bacteris acètics com Gluconobacter i Acetobacter, que utilitzen l’etanol generat com a font de carboni, oxidant-lo a àcid acètic.
La major part de l’àcid acètic present al vi es produeix durant la fermentació alcohòlica, i és subproducte del metabolisme dels llevats durant la transformació dels sucres en etanol. En poques paraules, no és possible fabricar vi sense generar una mica d’àcid acètic. Aquest procés és particularment intens a l’inici de la fermentació i després, una altra vegada, sobre el final de la fermentació. Està comprovat que l’àcid acètic, juntament amb el glicerol, són produïts pel metabolisme de Saccharomyces cerevisae per mantenir equilibrat el balanç redox, com a resposta davant de situacions d’estrès hiperosmòtic (a causa d’altes concentracions de sucres). Tot i que els nivells d’àcid acètic generats són normalment inferiors a 0,400,50 g/L, el contingut exacte pot variar força en funció de: el cep de Saccharomyces, la temperatura, el nivell de sucres, el nivell de nitrogen disponible, l’addició de vitamines i el pH.
Hi ha altres mecanismes de producció d’àcid acètic relacionats amb el creixement no controlat de determinats microorganismes capaços de produir-lo en quantitats considerables. Dins d’ells, es poden trobar bacteris acètics aerobis del gènere Acetobacter o Gluconobacter, bacteris làctics com Oenococcus i poblacions de llevats com Picchia, Candida, Kloeckera, Dekkera o Brettanomyces (particularment en condicions aeròbies). Per poder combatre aquests microorganismes cal reforçar les tasques d’higiene i desinfecció al celler, a més d’aplicar protocols amb SO2 i vigilar paràmetres fonamentals com ara pH i temperatura. A més, cal tenir en compte que els bacteris acètics són aerobis, és a dir que per créixer necessiten la presència d’oxigen. En aquests casos, un maneig correcte de les aportacions d’oxigen durant el procés serà fonamental per mantenir els valors d’acètic i volàtil dins dels marges tolerables. Durant la fermentació alcohòlica és senzill desplaçar l’oxigen gràcies a la producció de CO2, però després cal mantenir l’aportació als nivells més baixos possibles.
Seguint amb el procés de fabricació d’un vi, els bacteris làctics poden contribuir a apujar el nivell d’acètic al vi mentre es desenvolupa la fermentació malolàctica. Durant la descarboxilació de l’àcid màlic a làctic, els bacteris làctics heterofermentatius com Oenococcus oeni o Lactobacillus plantarum poden produir lleugeres quantitats d’acètic a l’ordre de 0,050,30 g/L, a partir de petites quantitats residuals de glucosa. Els nivells finals dependran de l’ús de bacteris comercials o nadius i de la competència entre aquests microorganismes.
Finalment, en el període d’emmagatzematge del vi, aquest tampoc no estarà fora de perill de patir augments en la concentració d’àcid acètic. Qualsevol població de bacteris acètics que hagi pogut sobreviure a la fermentació alcohòlica i malolàctica pot trobar les condicions necessàries per créixer i generar àcid acètic a partir de l’oxidació de l’etanol. En aquests casos caldrà reduir al màxim les aportacions d’oxigen que puguin venir de les diferents operacions de transvasament, clarificació, tràfecs, criança en barrica, filtració i embotellat. Serà important, per tant, reduir les maniobres amb el vi, evitar la utilització de tancs d’emmagatzematge i barriques que presentin aire als espais capdavanters, utilitzar gasos inerts per desplaçar l’oxigen sempre que sigui necessari i tenir un embotellament eficient que redueixi el aportació d’oxigen.
Quan i com es pot mesurar l’àcid acètic?
Com hem vist, els nivells d’àcid acètic es poden disparar en qualsevol moment del procés de producció. Per tant, és aconsellable mesurar aquest paràmetre almenys en els casos següents:
• Després de la fermentació alcohòlica.
• Després de la fermentació malolàctica.
• Durant les parades de fermentació.
• Periòdicament, durant l’emmagatzematge del vi.
• Quan els tancs no estan completament plens.
• Quan s’observa la presència d’un biofilm (de bacteris o llevats).
• Abans de l’embotellament.
Convé portar un registre de tots aquests valors, per poder detectar i solucionar un problema de manera ràpida i eficaç.
A l’hora de dur a terme la determinació, els laboratoris més tradicionals se solen decantar per mesurar l’acidesa volàtil, mentre que als més moderns s’ha imposat el mesurament de la concentració d’àcid acètic.
Mesurament de l’acidesa volàtil
Per mesurar l’acidesa volàtil, se solen utilitzar destil·ladors de vidre on l’escalfament s’efectua de manera indirecta fent servir vapor d’aigua. Per dur a terme correctament la mesura cal, en primer lloc, treure el diòxid de carboni de la mostra. També s’haurà de determinar de manera separada la contribució a l’acidesa del diòxid de sofre lliure i combinat que es pogués destil·lar juntament amb els àcids volàtils, de l’àcid sòrbic present (si s’hagués afegit al vi durant el procés de fabricació) i de l’àcid salicílic (si es va utilitzar com a conservant de la mostra de vi). Quant a l’aigua per generar el vapor, cal anar amb compte que sigui destil·lada i lliure de diòxid de carboni. Pel que fa a l’equip per destil·lar la mostra, consta bàsicament d’un generador de vapor, un baló per a la mostra, una columna de destil·lació i un condensador. No qualsevol equip pot ser utilitzat, segons l’OIV aquest ha de passar per 3 tipus de test perfectament detallats a la normativa (OIVMAAS31302) per assegurar que:
• El vapor d’aigua estigui lliure de diòxid de carboni, per a la qual cosa es destil·larà una mostra d’aigua bullida.
• Es recupera almenys el 99,5% de l’àcid acètic, per això es destil·la una mostra de solució d’àcid acètic 0,1M.
• No més d’un 0,5% de l’àcid làctic és destil·lat a la mostra, per a això es duu a terme una destil·lació d’una mostra de solució d’àcid làctic 1M.
D’acord amb la normativa OIV, cal utilitzar un volum de mostra de 20 mL de vi acidificat amb 0,50 g d’àcid tartàric, i s’han de recuperar uns 250 mL de destil·lat (aproximadament 6 minuts). Aquest destil·lat ha de ser després valorat utilitzant una solució d’hidròxid de sodi (0,1 M) i fenolftaleïna com a indicador.
Aquest tipus de mètodes solen ser tediosos i lents, i poden tenir diverses fonts d’error a causa de fuites a les unions, pèrdues de mostra i altres errors operatius. No obstant això, a molts països, està adoptat com a mètode oficial ia més està molt estès a cellers.

FOTO: Destil·lador DE 2000.

FOTO: Refrigerador d’aigua DE-Cooler.
Una solució ràpida i automatitzada per a aquest tipus d‟anàlisi seria utilitzar un destil·lador automàtic com el DE2000 comercialitzat per TDI, de màxima fiabilitat. A més, per a aquells usuaris preocupats pel consum d’aigua necessària per a la refrigeració, hi ha la possibilitat d’afegir una unitat de refrigeració de circuit tancat com el DECooler, comercialitzat també per TDI, que permet operacions de treball més respectuoses i sostenibles amb el medi ambient.
Mesurament de l’àcid acètic
La irrupció dels analitzadors automàtics ha modificat la manera de controlar la qualitat d’un vi. La tecnologia disponible avui en dia permet analitzar diversos paràmetres sobre un gran nombre de mostres en molt poc temps.

FOTO: Analitzador Miura One.

FOTO: Analitzador químic Miura 200.

FOTO: Analitzador químic Miura 200 2 braços.
A tall d’exemple, la gamma d’analitzadors Miura de TDI proporciona solucions d’anàlisi que van des de les 60 fins a les 220 determinacions per hora, augmentant l’eficiència i reduint costos al laboratori. Després de molts anys, la determinació d’àcid acètic en mostres de vi comença a ser observada com el mètode més econòmic i fiable de poder controlar l’evolució del vi, fins i tot sent avalada per diverses organitzacions.
El mètode de mesura es basa en l’acció d’un grup d’enzims que, de manera selectiva i molt específica, reaccionen amb l’àcid acètic i generen un canvi en l’absorbància a 340 nm, que és fàcil de monitoritzar mitjançant un detector. Amb l’ajuda d’un calibratge previ amb patrons de concentració coneguts, és possible determinar ràpidament la concentració d’àcid acètic en una mostra de vi incògnita.
A l’inici del desenvolupament d’aquestes tècniques, els kits enzimàtics per a la determinació d’àcid acètic estaven compostos per un gran nombre d’enzims i cofactors liofilitzats que s’havien de ressuspendre en tampons i que tenien una estabilitat relativament baixa. Tot això feia l’anàlisi enzimàtica poc pràctica i tediosa. Gràcies a la inversió en R+D realitzada per TDI des dels seus inicis, avui dia aquests kits es presenten en format líquid, amb una durabilitat alta i amb reactius de treball senzills de preparar i amb estabilitat àmpliament millorada. Aquestes prestacions, sumades a l’existència de patrons multiparamètrics estables ia la disponibilitat de mostres víniques de referència, formen una combinació indispensable per assegurar i mantenir la qualitat dels mesuraments. És per aquestes raons per les quals el kit d’Àcid Acètic de TDI és any rere any el top de vendes i el paràmetre més avaluat a tots aquells cellers que confien en els nostres productes.
TDI es caracteritza per proveir la millor solució analítica, a mida de cada celler i laboratori enològic, i el millor servei i atenció al client. Si teniu alguna necessitat analítica i voleu saber com resoldre-la, poseu-vos amb nosaltres via email (info@t-d-i.es), xarxes socials o al web www.tdianalizadores.com i junts podrem trobar la millor solució.
Més de 35 anys d’experiència enològica ens avalen, no ho dubteu i sumeu-vos a l’enolució!











 Taula 1. Continguts màxims de SO2 Total (mg/L) permesos a la UE.
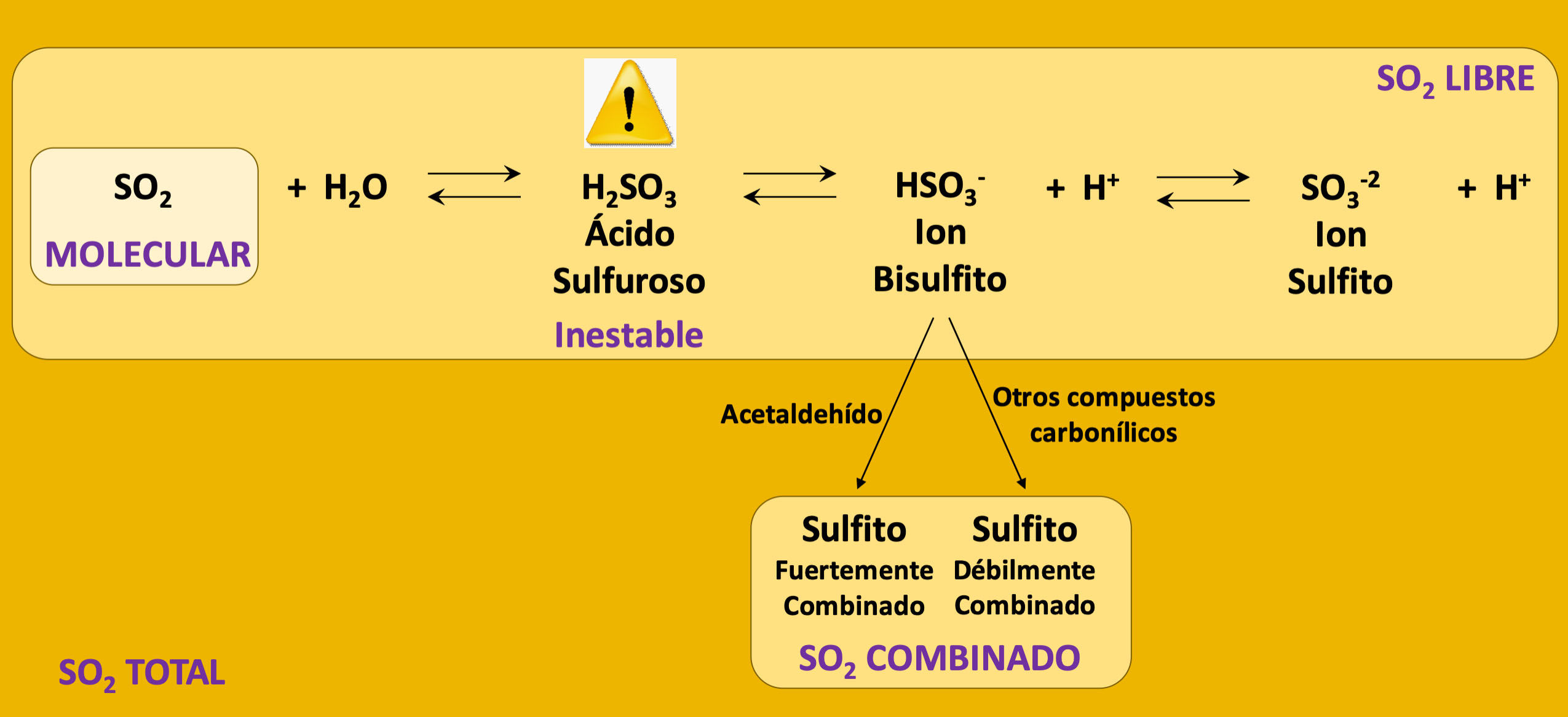
Taula 1. Continguts màxims de SO2 Total (mg/L) permesos a la UE. Figura 1. Equilibri esquemàtic de les formes químiques del SO2 presents al vi.
Figura 1. Equilibri esquemàtic de les formes químiques del SO2 presents al vi.